
1、行业主管部门和监管体制
医疗器械行业主要行业主管部门及行业协会为:
(1)国家发展和改革委员会:负责拟订并组织实施产业政策和价格政策;监督检查产业政策、价格政策的执行。推进产业结构战略性调整和升级;提出国民经济重要产业的发展战略和规划等。
(2)国家卫生和计划生育委员会:负责拟订卫生和计划生育事业中长期发展规划。拟订医疗机构、医疗技术应用、医疗质量、医疗安全、医疗服务、采供血机构管理等有关政策规范、标准并组织实施,参与药品、医疗器械临床试验管理工作。拟订卫生和计划生育科技发展规划及相关政策,组织实施相关科研项目、新技术评估管理、科研基地建设。
(3)国家食品药品监督管理总局:负责组织制定、公布药品和医疗器械标准、分类管理制度并监督实施。负责制定药品和医疗器械研制、生产、经营、使用质量管理规范并监督实施。负责药品、医疗器械注册并监督检查。建立药品不良反应、医疗器械不良事件监测体系,并开展监测和处置工作。
(4)中国医疗器械行业协会:是行业内从事相关工作的单位或个人在自愿的基础上联合组成的全国范围的行业性非盈利社会组织,其下属的体外诊断(IVD)分会主要职能包括提供行业权威信息和观点,引导行业活动;向相关政府及有关部门反映专委会成员意见,提出政策、立法、重大改革的意见和建议;在行业内开展理论研究、组织专家调研和经验交流活动;编辑、出版行业研究报告等。
由于医疗器械直接影响使用者的生命、健康和安全,医疗器械行业受到严格的行业监管。行业监管主要包括产品和企业两个方面:
(1)对产品的管理
我国对包括体外诊断试剂在内的医疗器械产品进行分类管理。
根据《医疗器械监督管理条例》(2000 年1 月4 日中华人民共和国国务院令第276 号公布,2014 年2 月12 日国务院第39 次常务会议修订通过,根据2017年5 月4 日《国务院关于修改〈医疗器械监督管理条例〉的决定》修订(国务院令第680 号)),我国对医疗器械按照风险程度分三类进行管理。
根据《医疗器械注册管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第4 号),我国对第一类医疗器械进行备案管理,对第二类、第三类医疗器械进行注册管理。
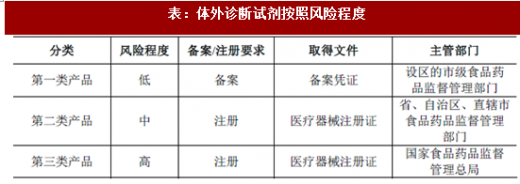
根据《体外诊断试剂注册管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第5 号),我国将体外诊断试剂按照风险程度划分为三类产品,并对备案和注册管理进行了具体规定。
(2)对企业的管理
我国对医疗器械生产和经营企业分别按规定进行分类管理。
①医疗器械生产企业
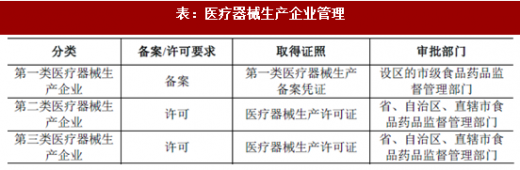
根据《医疗器械生产监督管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第7 号),我国对第一类医疗器械的生产企业进行备案管理,对第二、第三类医疗器械的生产企业进行许可管理。
②医疗器械经营企业
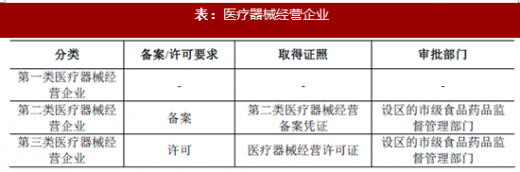
根据《医疗器械经营监督管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第8 号),第一类医疗器械的经营企业不需许可和备案,对第二类医疗器械的经营企业进行备案管理,对第三类医疗器械的经营企业进行许可管理。
2、行业主要法律法规及政策
与体外诊断试剂及其所属医疗器械行业直接或间接相关的主要法律、法规、政策、标准及其相关具体内容如下:
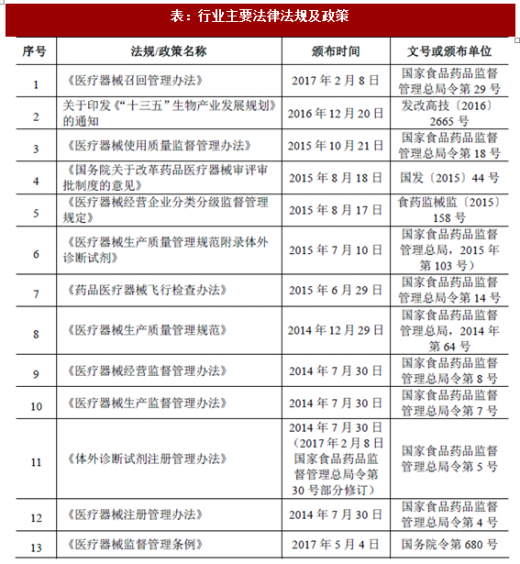
(1)《医疗器械召回管理办法》(2017 年2 月8 日国家食品药品监督管理总局令第29 号)
规定医疗器械生产企业应当按照本办法的规定建立健全医疗器械召回管理制度,收集医疗器械安全相关信息,对可能的缺陷产品进行调查、评估,及时召回缺陷产品。医疗器械经营企业、使用单位应当积极协助医疗器械生产企业对缺陷产品进行调查、评估,主动配合生产企业履行召回义务,按照召回计划及时传达、反馈医疗器械召回信息,控制和收回缺陷产品。
(2)关于印发《“十三五”生物产业发展规划》的通知(2016 年12 月20日发改高技〔2016〕2665 号)
要求推动重点领域新发展,提升生物医学工程发展水平,提供快速准确便捷检测手段,包括针对急性细菌感染、病毒感染等重大传染性疾病,包括外来重大传染性疾病的检测需求,加速现场快速检测的体外诊断仪器、试剂和试纸的研发和产业化。
(3)《医疗器械使用质量监督管理办法》(2015 年10 月21 日国家食品药品监督管理总局令第18 号)
要求医疗器械生产经营企业销售的医疗器械应当符合强制性标准以及经注册或者备案的产品技术要求。医疗器械生产经营企业应当按照与医疗器械使用单位的合同约定,提供医疗器械售后服务,指导和配合医疗器械使用单位开展质量管理工作。
参考观研天下发布《2018年中国医疗器械行业分析报告-市场运营态势与投资前景预测》
(4)《国务院关于改革药品医疗器械审评审批制度的意见》(2015 年8 月18日国发〔2015〕44 号)
提出改革医疗器械审批方式。鼓励医疗器械研发创新,将拥有产品核心技术发明专利、具有重大临床价值的创新医疗器械注册申请,列入特殊审评审批范围,予以优先办理。及时修订医疗器械标准,提高医疗器械国际标准的采标率,提升国产医疗器械产品质量。通过调整产品分类,将部分成熟的、安全可控的医疗器械注册审批职责由食品药品监管总局下放至省级食品药品监管部门。
(5)《医疗器械经营企业分类分级监督管理规定》(2015 年8 月17 日食药监械监〔2015〕158 号)
将医疗器械经营企业分为三个监管级别。其中三级监管为风险最高级别的监管,主要是对医疗器械经营环节重点监管目录涉及的经营企业,为其他医疗器械生产经营企业提供贮存、配送服务的经营企业,上年度存在行政处罚且整改不到位和存在不良信用记录的经营企业进行的监管。二级监管为风险一般级别的监管,主要是对除三级监管外的经营第二、三类医疗器械的批发企业进行的监管。
一级监管为风险较低级别的监管,主要是对除二、三级监管外的其他医疗器械经营企业进行的监管。医疗器械经营企业涉及多个监管级别的,按最高级别对其进行监管。
(6)《医疗器械生产质量管理规范附录体外诊断试剂》(2015 年7 月10 日,2015 年第103 号)
附录是对体外诊断试剂生产质量管理规范的特殊要求。体外诊断试剂生产质量管理体系应当符合《医疗器械生产质量管理规范》及附录的要求。
(7)《药品医疗器械飞行检查办法》(2015 年6 月29 日国家食品药品监督管理总局令第14 号)
飞行检查是食品药品监督管理部门针对药品和医疗器械研制、生产、经营、使用等环节开展的不预先告知的监督检查。办法规定了飞行检查的启动、实施检查和处理的相关内容,包括可以展开飞行检查的情形,检查组的记录、抽检、采取行政强制措施及采取风险控制措施的情形。根据飞行检查结果,食品药品监督管理部门可以依法采取限期整改、发告诫信、约谈被检查单位、监督召回产品、收回或者撤销相关资格认证认定证书,以及暂停研制、生产、销售、使用等风险控制措施。
(8)《医疗器械生产质量管理规范》(2014 年12 月29 日国家食品药品监督管理总局,2014 年第64 号)
目的为保障医疗器械安全、有效,规范医疗器械生产质量管理。医疗器械生产企业在医疗器械设计开发、生产、销售和售后服务等过程中应当遵守。企业应当结合产品特点,建立健全与所生产医疗器械相适应的质量管理体系,并保证其有效运行。将风险管理贯穿于设计开发、生产、销售和售后服务等全过程,所采取的措施应当与产品存在的风险相适应。
(9)《医疗器械经营监督管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第8 号)
按照医疗器械风险程度,医疗器械经营实施分类管理。经营第一类医疗器械不需许可和备案,经营第二类医疗器械实行备案管理,经营第三类医疗器械实行许可管理。其中,从事第三类医疗器械经营的,经营企业应当向所在地设区的市级食品药品监督管理部门提出申请;符合规定条件的,依法许可并发给《医疗器械经营许可证》;证书有效期为5 年,有效期届满需要延续的,应在规定时间内向有权部门提出延续申请。从事第二类医疗器械经营的,经营企业应当向所在地设区的市级食品药品监督管理部门备案;食品药品监督管理部门对符合规定的予以备案,发给第二类医疗器械经营备案凭证。
(10)《医疗器械生产监督管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第7 号)
开办第二类、第三类医疗器械生产企业的,应当向所在地省、自治区、直辖市食品药品监督管理部门申请生产许可;符合规定条件的,依法许可并发给《医疗器械生产许可证》,证书有效期为5 年,有效期届满需要延续的,应在规定时间内向有权部门提出延续申请。开办第一类医疗器械生产企业的,应当向所在地设区的市级食品药品监督管理部门办理第一类医疗器械生产备案;食品药品监督管理部门对符合规定条件的予以备案,发给第一类医疗器械生产备案凭证。
(11)《体外诊断试剂注册管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第5 号,2017 年2 月8 日国家食品药品监督管理总局令第30 号部分修订)
按医疗器械管理的体外诊断试剂,包括在疾病的预测、预防、诊断、治疗监测、预后观察和健康状态评价的过程中,用于人体样本体外检测的试剂、试剂盒、校准品、质控品等产品,可以单独使用,也可以与仪器、器具、设备或者系统组合使用。办法不包括按照药品管理的用于血源筛查的体外诊断试剂和采用放射性核素标记的体外诊断试剂。
第一类体外诊断试剂实行备案管理,第二类、第三类体外诊断试剂实行注册管理。境内第一类体外诊断试剂备案,备案人向设区的市级食品药品监督管理部门提交备案资料。境内第二类体外诊断试剂由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。境内第三类体外诊断试剂由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
根据产品风险程度由低到高,体外诊断试剂分为第一类、第二类、第三类产品。其中,第一类产品:1、微生物培养基(不用于微生物鉴别和药敏试验);2、样本处理用产品,如溶血剂、稀释液、染色液等。第二类产品:除已明确为第一类、第三类的产品,其他为第二类产品。第三类产品:1、与致病性病原体抗原、抗体以及核酸等检测相关的试剂;2、与血型、组织配型相关的试剂;3、与人类基因检测相关的试剂;4、与遗传性疾病相关的试剂;5、与麻醉药品、精神药品、医疗用毒性药品检测相关的试剂;6、与治疗药物作用靶点检测相关的试剂;7、与肿瘤标志物检测相关的试剂;8、与变态反应(过敏原)相关的试剂。
(12)《医疗器械注册管理办法》(2014 年7 月30 日国家食品药品监督管理总局令第4 号)
第一类医疗器械实行备案管理。第二类、第三类医疗器械实行注册管理。境内第一类医疗器械备案,备案人向设区的市级食品药品监督管理部门提交备案资料。境内第二类医疗器械由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。境内第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。医疗器械注册证有效期为5 年。
(13)《医疗器械监督管理条例》(2017 年5 月4 日国务院令第680 号)
国家对医疗器械按照风险程度实行分类管理。第一类是风险程度低,实行常规管理可以保证其安全、有效的医疗器械。第二类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械。第三类是具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械。第一类医疗器械产品备案,不需要进行临床试验。申请第二类、第三类医疗器械产品注册,应当进行临床试验,规定免于进行临床试验的医疗器械除外。
资料来源:观研天下整理,转载请注明出处。